Primeira vacina aprovada no mundo contra o vírus VRSH, uma das causas de doenças como bronquiolite e pneumonia
 |
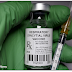
| Vacina Arexvy, contra o vírus VRSH, desenvolvida pela companhia farmacêutica GSK. |
A Administração de Drogas e Alimentos dos EUA (FDA) aprovou a vacina desenvolvida pela companhia GSK, Arexvy, contra o vírus respiratório sincicial humano (VRSH) e para uso em pessoas com 60 anos ou mais de idade (Ref.1). Essa é a primeira vacina contra o VRSH a ganhar aprovação no mundo - um feito recebido com grande comemoração pela comunidade médica (Ref.2). Esse vírus geralmente causa sintomas leves como aqueles observados durante um resfriado comum. Porém, para indivíduos idosos, pode ser letal, além de ser uma importante causa de mortalidade infantil.
O VSRH é um vírus altamente contagioso e pertence à família Paramyxoviridae, do gênero pneumovírus. Envolvido com um genoma de RNA de cadeia simples e de sentido negativo, esse vírus é constituído por uma bicamada lipídica, e tem em sua estrutura as glicoproteínas F, a qual realiza ligação viral e medeia o processo de fusão entre o vírus e as membranas celulares do hospedeiro, formando um sincício, e a proteína G que participa da adesão entre o vírus e a célula do hospedeiro.
 |
| Na imagem, obtida via micrografia eletrônica, uma partícula viral do vírus VSRH emergindo de uma célula infectada. |
As infecções agudas do trato respiratório inferior (IATRIs) são caracterizadas por processos inflamatórios agudos, infecciosos ou não, acometendo alvéolos, bronquíolos, brônquios e espaço intersticial. Essas doenças são responsáveis por altos índices de morbidade e mortalidade infantil em todo o mundo, representando a primeira causa de mortes nos países de baixa renda e a quarta nos países de média renda, que incluem o Brasil.
Dentre os vários agentes etiológicos causadores de IATRI, os vírus são responsáveis por bronquiolite (inchaço das pequenas vias aéreas nos pulmões) e pneumonia (infecção que inflama os sacos de ar em um ou ambos os pulmões, que podem ficar cheios de líquido), as quais podem ser particularmente fatais para bebês e pessoas com mais de 65 anos. Com distribuição mundial, o vírus VSRH é o principal agente de IATRIs a nível global, sendo responsável por até >80% dos casos de bronquiolite viral aguda (BVA). No Brasil, o VSRH é responsável por 64% dos pacientes internados com BVA (Ref.4).
A infecção pelo VSRH apresenta caráter sazonal, com predominância entre o período do outono e o inverno. A transmissão se faz pelo contato direto com as secreções respiratórias e pelo contato indireto, de objetos e superfícies contaminadas, podendo sobreviver por até 24 horas. A transmissibilidade inicia-se 2 dias antes do aparecimento dos sinais e sintomas, sendo que, a disseminação pode persistir por até 4 semanas. A infecção ocorre quando o vírus atinge as mucosas conjuntivas da orofaringe e da nasofaringe, além de ser transmitido pela inalação de gotículas eliminadas através de tosses ou espirros de pessoas infectadas.
A ocorrência de surtos causados pelo VSRH acontece tanto nas comunidades como em ambientes hospitalares, principalmente dentro das Unidades de Terapia Intensiva (UTI) Neonatal e Pediátrica.
Mas além da óbvia preocupação pediátrica, as doenças causadas pelo VSRH impactam de forma séria a população idosa. Segundo o Centro de Controle e Prevenção de Doenças dos EUA (CDC), anualmente infecções por esse vírus causam a morte de aproximadamente 6-10 mil adultos nos EUA com 65 anos ou mais de idade, além de causar a hospitalização de 60 mil a 120 mil pessoas nessa faixa de idade. Indivíduos idosos com comorbidades como doença pulmonar obstrutiva crônica, asma e insuficiência cardíaca, e/ou com sistema imune enfraquecido, estão em especial risco de progressão severa.
A vacina da GSK aprovada esta semana de forma inédita no mundo, chamada Arexvy, é baseada na proteína F (forma pré-fusão) do subgrupo A do VSRH - um dos dois subtipos do vírus (o outro é o VSRH-B). Essa proteína (antígeno) é então associada com um adjuvante para otimizar o reconhecimento pelas células imunes do corpo e aumentar a produção de anticorpos neutralizantes contra o vírus. Por enquanto a vacina foi aprovada apenas nos EUA, mas em breve é aguardada aprovação também na Europa.
A aprovação do FDA para a Arexvy foi suportada em especial pelos resultados de um robusto estudo clínico de Fase III ainda em andamento e publicado este ano no periódico The New England Journal of Medicine (Ref.5). No estudo, aproximadamente 12,5 mil participantes receberam o imunizante (dose única) e 12,5 mil participantes receberam um placebo. Entre os participantes que receberam o imunizante e acompanhados por uma média de 6,7 meses, o risco de IATRIs causada por VSRH foi reduzido em 82,6% e o risco de desenvolver uma forma severa de IATRI causada por VSRH foi reduzido em 94,1%. A eficácia mostrou-se similar em relação aos dois subtipos do vírus (A e B).
A vacina mostrou-se segura, com incidência de sérios efeitos adversos similar entre o grupo recebendo o imunizante e o grupo recebendo placebo. Efeitos adversos leves a moderados foram observados com maior frequência no grupo recebendo o imunizante, comumente incluindo dor no local da injeção, fatiga, dor muscular, dor de cabeça e dor/rigidez nas articulações.
É esperado que em breve o FDA aprove também vacinas similares (proteína F-baseadas) das companhias farmacêuticas Pfizer e Moderna para adultos com 60 anos ou mais e para mulheres grávidas, nesse último caso visando especificamente reduzir o risco de infecção ou progressão severa de doença pulmonar em bebês. Um estudos clínico de Fase III publicado também este ano no The New England Journal of Medicine (Ref.6) encontrou que o risco de IATRI severa em bebês com até 90 dias de idade cujas mães receberam o imunizante durante a gravidez foi reduzido em quase 82%. O sistema imune de recém-nascidos não responde de forma robusta a várias vacinas administradas de forma direta; a estratégia de imunizar as grávidas acaba sendo uma melhor estratégia nesse sentido.
Todos os anos, 58 mil a 80 mil crianças nos EUA com 5 anos de idade ou menos são hospitalizadas devido a infecção pelo VSRH, com 100 a 300 mortes resultantes de acordo com o CDC Norte-Americano.
REFERÊNCIAS
- https://www.fda.gov/news-events/press-announcements/fda-approves-first-respiratory-syncytial-virus-rsv-vaccine
- https://www.nature.com/articles/d41586-023-01529-5
- https://www.scielo.br/j/jped/a/NPLtc7SMqbXgynmkV4gtmRH/
- https://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1699-714X2020000100010
- https://www.nejm.org/doi/10.1056/NEJMoa2209604
- https://www.nejm.org/doi/10.1056/NEJMoa2216480
 Reviewed by Saber Atualizado
on
maio 04, 2023
Rating:
Reviewed by Saber Atualizado
on
maio 04, 2023
Rating:












